مسیرهاي فرآیند
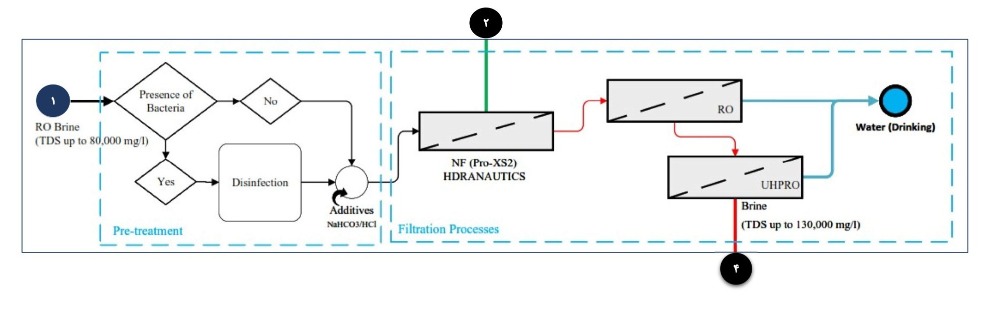
در فرآیند فیلتراسیون
- پس از گندزدایی پساب، با استفاده از نانوفیلتر تجاري NF-Pro-XS2، آب موجود در پساب را تا حدود 30 درصد ریکاوري میکنیم. این فرآیند باعث تغلیظ سازي پساب حاوي یونهاي دوظرفیتی کلسیم و منیزیم و آنیونهاي کربنات و سولفات خواهد شد )پساب نانوفیلترها در مسیر 2(.
- با توجه به اطلاعات فنی این نانوفیلترها، پس از تنظیم pH پساب اولیه، تا حدود 99.8 درصد حذف یونهاي دوظرفیتی نظیر +Mg2 و -SO42، و کمتر از 10 درصد حذف یونهاي تکظرفیتی نظیر +Na و -Cl را خواهیم داشت. از این رو با استفاده از این روش، بیش از 90 درصد یونهاي تکظرفیتی از نانوفیلتر عبور کرده و پس از تغلیظسازي توسط فیلتراسیون اسمز معکوس با فشار پایین )RO( و بالا )UHP-RO(، وارد مسیر 4 میشوند.
در کنار جدایش یونی در فرآیند فیلتراسیون، تولید محصول جانبی آب شیرین را نیز خواهیم داشت.
فرآیند استحصال منیزیم و تولید ترکیبات منیزیم-کلسیمی نظیر دولومیت از پساب نانوفیلترها مسیر سبزرنگ 2
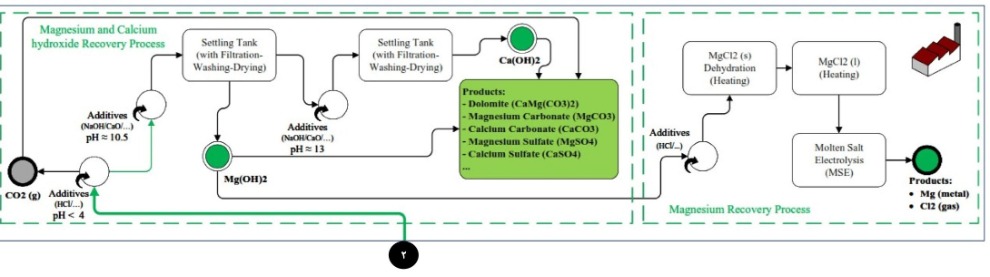
- با توجه به غلظت بالاي یون فلزي منیزیم در این پساب )به عنوان دومین یون فلزي با غلظت بالا بعد از سدیم(، میتوان از این پساب براي تولید منیزیم پودري و
اکسید منیزیم استفاده کرد.
- به طور کلی در روش پیشنهادي از یک سل الکترولیز حاوي MgCl2 به همراه ترکیبات کلریدي هدایتسازهاي نظیر CaCl2 و NaCl و KCl استفاده میشود. با توجه به درصد ریکاوري نانوفیلترها، در پساب خروجی از این فیلتراسیون کلیهي یونهاي مورد نیاز براي این فرآیند با غلظت بیشتر کلسیم و منیزیم در ترکیب خروجی حضور خواهند داشت، که به استحصال الکترولیزي منیزیم کمک خواهند کرد.
- از این روش صنعتی، با صرف انرژي حرارتی در کورههاي ذوب و انرژي الکتریکی در سل الکترولیز مذاب منیزیم کلراید، میتوان جهت تولید منیزیم با خلوص بالا پس از مراحل تهنشینسازي از الکترولیتهاي حاوي یونهاي منیزیم نظیر پسابهاي صنعتی استفاده کرد.
اما، پیش از اینکه بتوان از این پساب جهت استحصال منیزیم استفاده کرد، باید ابتدا یونهاي منیزیم را از کلسیم جدا کنیم. از این جهت، نیازمند فرآیند ترسیب دو مرحلهاي جهت تولید منیزیمهیدروکسید و کلسیمهیدروکسید خواهیم بود.
از اینرو، به منظور تشکیل رسوبات هیدروکسیدکلسیم و هدروکسیدمنیزیم از روش جدایش دو مرحلهاي توسط تغییرات pH استفاده خواهد شد. حضور این Pre-Treatment در مسیر پیشنهادي، سبب افزایش خلوص محصول نهایی منیزیم پس از الکترولیز نمک مذاب منیزیم کلراید خواهد شد. این
پیش فرآیند در مرحلهي Magnesium and Calcium Hydroxide Recovery و با توجه به شماتیک زیر صورت خواهد گرفت.
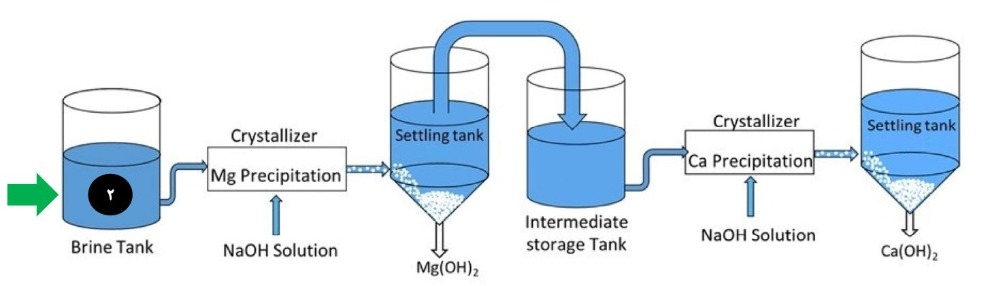
- از ترکیبات هیدروکسیدي تشکیل شده، میتوان در ابتدا براي تشکیل محصولاتی نظیر دولومیت، کلسیتهاي پرمنیزیم و تولید سولفات منیزیم با خلوص بالا
استفاده کرد.
- از طرفی میتوان از هیدروکسیدمنیزیم )2)Mg(OH( تولیدي به عنوان خوراك اصلی واحدهاي استحصال منیزیم توسط فرآیند الکترولیزي مذاب کلریدمنیزیم استفاده کرد. این روش، به عنوان رایجترین روش تولید منیزیم در کشورهاي پیشرفتهاي نظیر امریکا و روسیه جهت استحصال این فلز ارزشمند، استفاده میشود.
فرآیند استحصال منیزیم )Dow Process – (Magnesium Recovery Process فرآیند تولید منیزیم به روش الکترولیز نمک مذاب MgCl2 در دو مرحلهي کلی صورت میگیرد:
1. دهیدراته کردن منیزیم کلراید
با استفاده از روش جایگزینی در اثر افزودن محلول آبی HCl به رسوب تولیدي 2)Mg(OH در فرآیند ترسیب منیزیم، محلول آبی MgCl2 تشکیل شده و سپس این محلول با توجه به محدودهي دمایی زیر دماي خروج T<140°C) HCl( حرارت داده و فرآیند Dehydration، در شرایط
کنترلی فوقالذکر انجام خواهد گرفت.
2. تبدیل منیزیم کلراید مذاب به منیزیم فلزي و گاز کلر در سل الکترولیز با آند گرافیتی در دماي 700°C
در سل الکترولیز در محفظه کاتد جهت جلوگیري از اکسیداسیون منیزیم از دمش گاز خنثی استفاده میشود.
محصول اصلی این فرآیند )منیزیم فلزي( در کاتد تشکیل میشود، و در انتها به صورت شمش به فروش میرسد.
محصول جانبی این فرآیند تولید گاز کلرخواهد بود، که میتوان از آن جهت تولید محصول نهایی اسید کلریدریک )HCl( استفاده نمود.
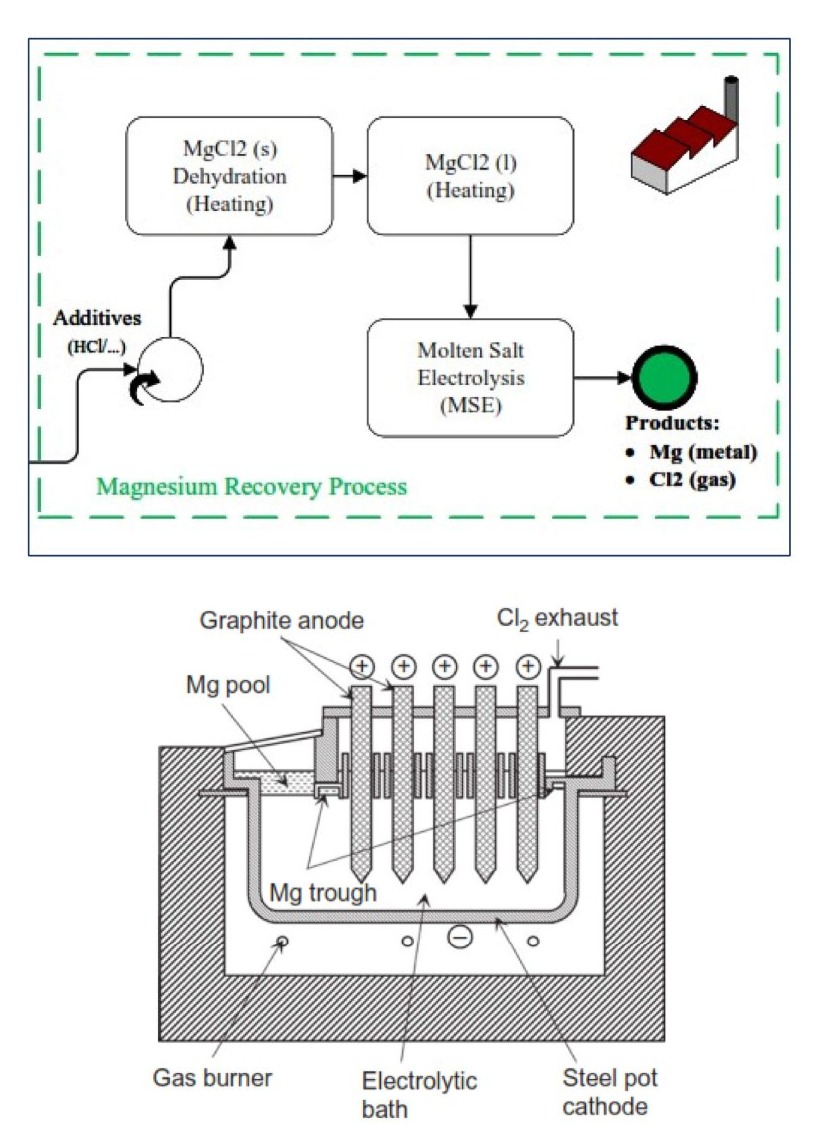
فرآیند استحصال منیزیم )Dow Process – (Magnesium Recovery Process پس از ترسیب منیزیمهیدروکسید )2)Mg(OH( در مرحله Pre-Treatment طراحی شده، و کلسینه کردن آن، میتوان به اکسیدمنیزیم )MgO( دست یافت.
- با تولید منیزیمهیدروکسید )2)Mg(OH( از پساب فوق، میتوان از آن به عنوان خوراك اصلی استحصال منیزیم توسط فرآیند Dow استفاده کرد. مراحل کلی این روش در فلودیاگرام فوق، به همراه نتایج عملیاتی روش Dow، جهت استحصال منیزیم از منیزیمهیدروکسید آورده شده است:

همانطور که در فرآیند شرح داده شده استحصال منیزیم از پساب RO )مسیر سبز رنگ خروجی 2(، نیاز به دو عامل سود )NaOH( و حرارت که گاز
هیدروژن )H2( به عنوان سوخت پاك میباشد، میتوان هر دوي این عوامل را از طریق فرآیند کلرآلکالین تهیه نمود. ضـمن اینکـه در فرآینـد جـدایش منیزیم از پساب، مقدار زیادي آب نمک تقریبا خالص جداسازي میشود که میتوان از این مایع )مسیر قرمز رنگ خروجی 4( براي فرآیند کلرآلکـالین
استفاده کرد و نیازي به استفاده از آب خام تصفیه شده در شرایط نرمال وجود نخواهد داشت.
 فرآیند کلرآلکالی - فناوري سل غشایی
فرآیند کلرآلکالی - فناوري سل غشایی
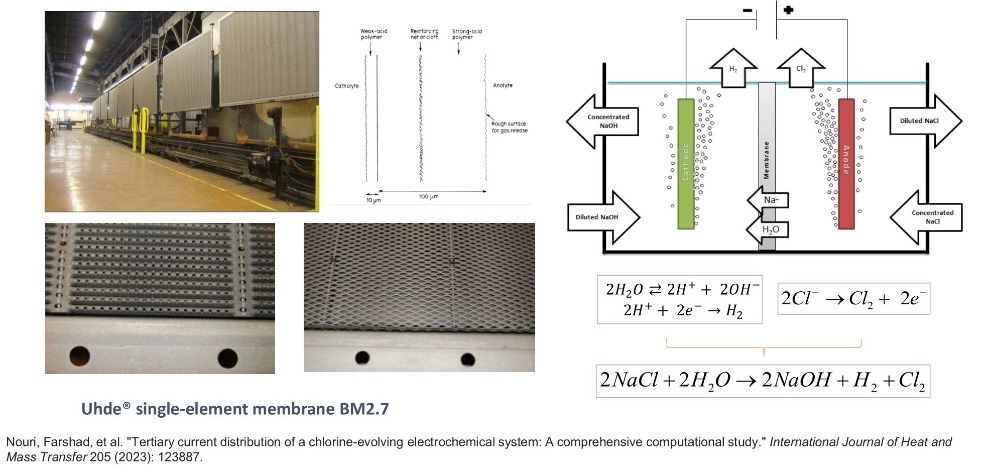 فلودیاگرام آمادهسازي آبنمک و فرآیند کلرآلکالی
فلودیاگرام آمادهسازي آبنمک و فرآیند کلرآلکالی
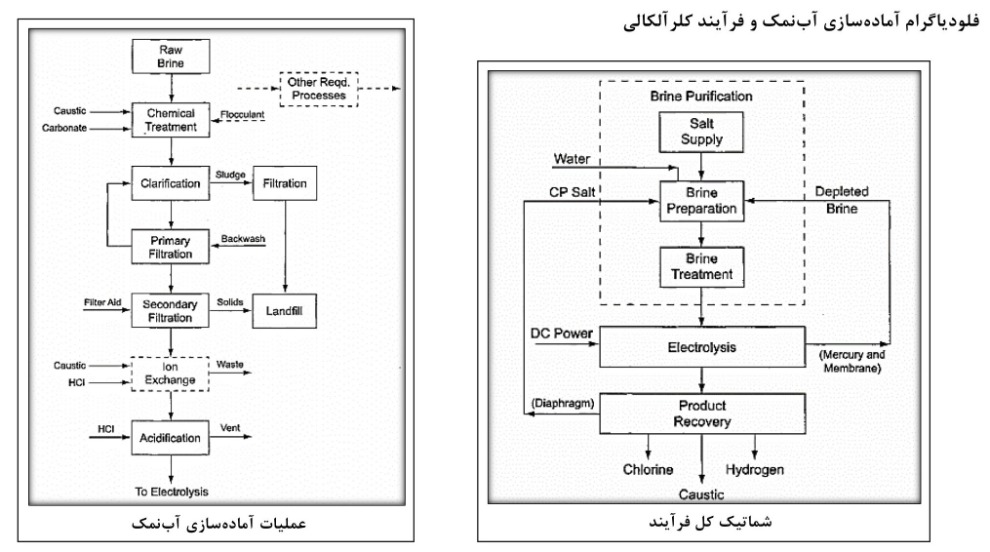 به عنوان یکی از محصولات قابل تولید از سود )NaOH( و کلر )Cl2( تولید شده در فرآیند کلرآلکالی، میتوان به آب ژاول )NaOCl( اشاره کرد.
به عنوان یکی از محصولات قابل تولید از سود )NaOH( و کلر )Cl2( تولید شده در فرآیند کلرآلکالی، میتوان به آب ژاول )NaOCl( اشاره کرد.
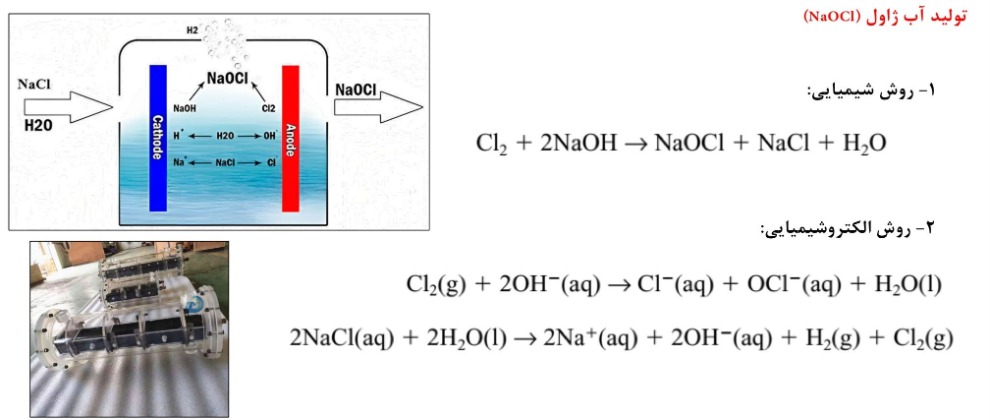
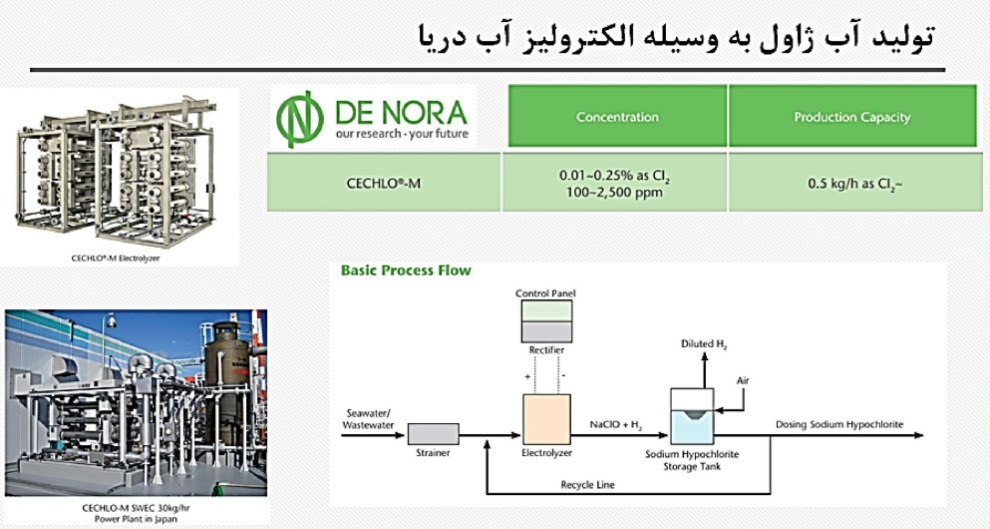
- از اینرو با توجه به مسیر فرآیندي ذکر شده، به طور خلاصه میتوان دو فرآیند اصلی استحصال منیزیم و کلرآلکالی را جهت تولید محصولات نهایی داشته باشیم.
- علت اساسی نیاز به تاسیس پلنت کلر آلکالی براي تامین HCl ،NaOH و نهایتا H2 به عنوان سوخت پاك و رایگان در فرآیند تولید منیزیم می باشد. بدیهی است ظرفیت مازاد این پلنت جهت درآمد جنبی، قابلیت عرضه به بازار داخلی و منطقه خلیج فارس را خواهد داشت.
بر اساس BFD کلی فوق نحوه ارتباط بین این دو فرآیند مشخص شده است:
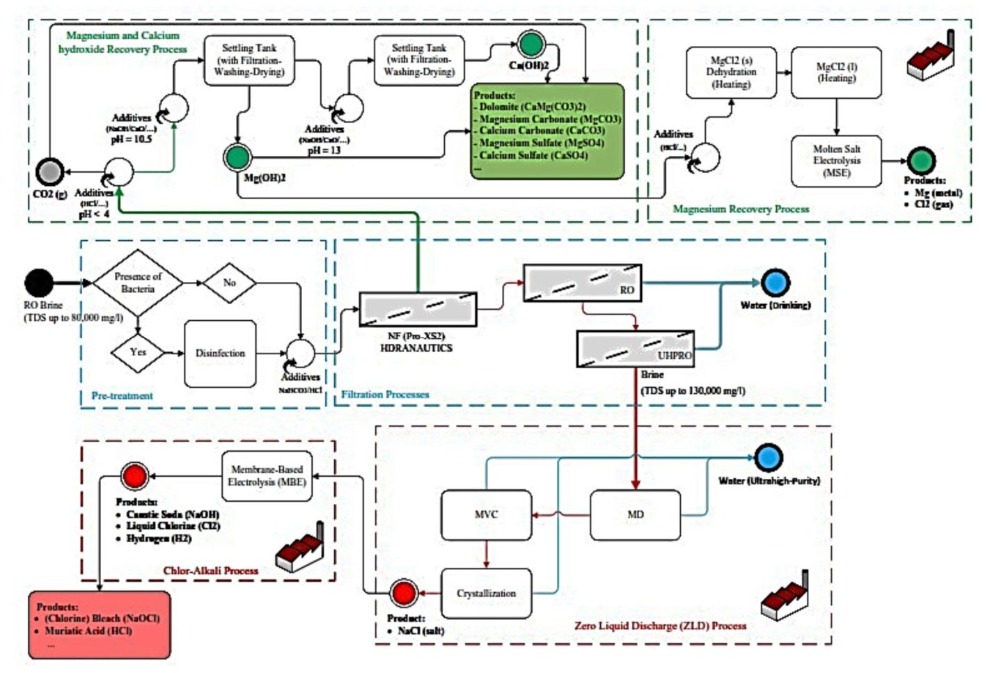
الف: ( محصولات پلنت منیزیم )Mg( در فرآیند استحصال منیزیم که عامل اصلی آن الکترولیز نمک مذاب MgCl2 است، محصولاتی مانند منیزیم و کلر تولید میشود، که پس از آن میتوان انواع مشـتقات جانبی را از این فرآیند تولید کرد. برخی از این مشتقات عبارتند از:
:(Mg) منیزیم
- تولید شمش و در فازهاي بعدي آلیاژ منیزیم،
- (MgO) تولید اکسیدمنیزیم
:(Cl) کلر
- (HCl) تولید اسید کلربدریک
- تولید کلروفریک
ب: محصولات پلنت کلرآلکالی
در فرآیند کلرآلکالی که عامل اصلی آن الکترولیز نمک محلول در آب است، محصولاتی مانند هیدروژن، سود و کلر تولید میشود، که پس از آن میتوان انـواع مشـتقات جانبی را از این فرآیند تولید کرد. برخی از این مشتقات عبارتند از:
:(Cl) کلر
-،(HCl) تولید اسید کلربدریک
-،(NaOCl) تولید آب ژاول
- تولید پرکلرین
-تولید کلروفریک
(H) هیدروژن
- (NaOH) سود سوزآور
-محصولات حاوي کلر
-منبع تولید انرژي پاك